
miércoles, 23 de septiembre de 2009
Modelos Atómicos
A través de la historia el hombre a tratado de describir las propiedades de la materia y de los que nos rodea de la mejor manera y sin dejar ningún factor de lado de tal manera que esta interpretación nos sirva de base para una estructura matemática que nos permita resolver problemas.


Modelo Atómico Matemático de Schrodinger y Heisenberg
Este modelo matemático no expresa claramente la posición de los electrones esta basado en los estudios de Mecánica Cuántica en la cual se plantea que los electrones se encuentran en determinadas regiones denominadas orbitales de tal manera que en esta región la probabilidad de localizar un electrón es máxima.
Este modelo se basa en la dualidad de la materia que se comporta como onda y partícula y en el principio de incertidumbre de Heisenberg que nos dice que es imposible determinar la velocidad y la posición de un electrón al mismo tiempo en un instante determinado.
Este modelo se basa en la dualidad de la materia que se comporta como onda y partícula y en el principio de incertidumbre de Heisenberg que nos dice que es imposible determinar la velocidad y la posición de un electrón al mismo tiempo en un instante determinado.
Heisenberg
En 1925, Heisenberg comenzó a desarrollar un sistema de mecánica cuántica, denominado mecánica matricial, en el que la formulación matemática se basaba en las frecuencias y amplitudes de las radiaciones absorbidas y emitidas por el átomo y en los niveles de energía del sistema atómico.Este modelo matemático no expresa claramente la posición de los electrones, este modelo esta basado en los estudios de Mecánica Cuántica en la cual se plantea que los electrones se encuentran en determinadas regiones denominadas orbitales de tal manera que en esta región la probabilidad de localizar un electrón es máxima.
Este modelo se basa en la dualidad de la materia que se comporta como onda y partícula y en el principio de incertidumbre de Heisenberg que nos dice que es imposible determinar la velocidad y la posición de un electrón al mismo tiempo en un instante determinado.

Este modelo se basa en la dualidad de la materia que se comporta como onda y partícula y en el principio de incertidumbre de Heisenberg que nos dice que es imposible determinar la velocidad y la posición de un electrón al mismo tiempo en un instante determinado.

Schrödinger

Ecuacion de ondas de Schrödinger:
Schrödinger formuló una ecuación llamada: ecuación de ondas de Schrödinger que describe el comportamiento y la energía de las partículas subatómicas. Esta ecuación
incluye el comportamiento de la partícula(m), como el de onda(Ψ)que depende de la ubicacion del sistema en el espacio.
Sin embargo, el nombre de "modelo atómico" de Schrödinger puede llevar a confusión ya que no explica la estructura completa del átomo. El modelo de Schrödinger explica sólo la estructura electrónica del átomo y su interacción con la estructura electrónica de otros átomos, pero no explica como es el núcleo atómico ni su estabilidad.

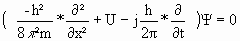

Modelo de la nube de electrones:
Según este modelo, los átomos metálicos ceden sus electrones de valencia a una "nube electrónica" que comprende todos los átomos del metal.Entonces el enlace metálico resulta de las atracciones electrostáticas entre los restos positivos y los electrones móviles que pertenecen en su conjunto a la red metálica.

Louis de Broglie
martes, 22 de septiembre de 2009
Bibliografia:
http://iesdolmendesoto.org/zonatic/el_enlace_quimico/enlace/enlace_metalico.html http://usuarios.lycos.es/billclinton/ciencia/modelos_atomicos.htm http://www.gobiernodecanarias.org/educacion/3/Usrn/lentiscal/1-CDQuimica-TIC/applets/Actual/teoriamodeloactual.htm
Suscribirse a:
Entradas (Atom)

